我院王文涛副教授(陈月琴团队)揭示H3K79me2指导mRNA“TWINS”区域m6A选择修饰介导蛋白翻译的新机制
m6A修饰是真核生物mRNA广泛存在的表观遗传修饰。m6A修饰功能强大且具有可逆性,参与了包括白血病发生发展在内的多种重要生物过程。m6A含量改变和m6A在底物RNA上的分布模式共同控制着RNA的命运。许多测序数据显示,m6A除了在RNA的终止密码子区域高峰富集,还会富集在起始密码子区域,且主要参与调控RNA翻译过程。然而,m6A修饰选择富集在起始密码子区域的调控机制还很大程度未知。

陈月琴/王文涛课题组联合中山大学附属第一医院黄礼彬课题组,在《The EMBO Journal》在线发表题为《RBM15B recognizes H3K79me2 to guide selective m6A-modification of mRNA and enhance oncoprotein translation in MLL-r leukemia》的研究成果。研究团队发现,m6A甲基转移酶复合物成员之一的RBM15B(RNA-binding motif protein 15B)可以作为一个遗传信息的传递者,选择性地调控起始密码子和靠近起始的部分编码区域的m6A修饰。研究团队将该区域定义为TWINS(two wings around start codon)。同时结合体内体外研究,也发现RBM15B能特异促进MLL-r白血病恶性进展。随后深入机制研究发现,RBM15B依赖其H47残基,可以直接识别组蛋白修饰H3K79me2,招募核心甲基转移酶METTL3对MLL融合蛋白下游靶标转录本的TWINS区域进行m6A修饰。受到H3K79me2-RBM15B axis调控的m6A修饰能进一步提高癌基因转录本的翻译效率,进而促进MLL-r白血病进程。这项研究不但揭示了一个之前未知的转录本TWINS区域的m6A选择修饰机制,也提示了RBM15B可作为恶性血液肿瘤中治疗靶标的可能性。此外,该项目工作提示H3K79me2不但具有转录调控功能,而且还能直接调控蛋白翻译。
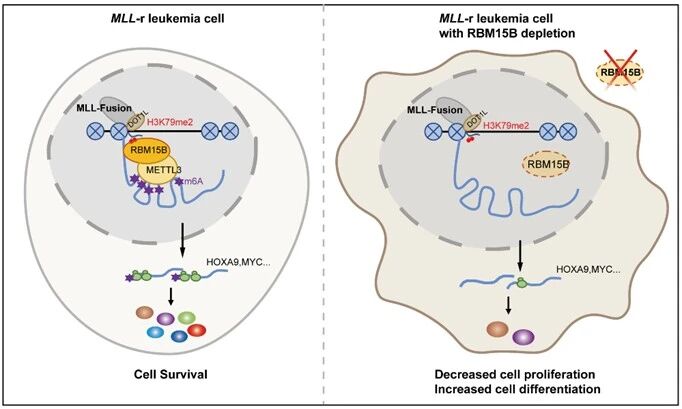
RBM15B识别H3K79me2调控m6A选择修饰的模式图
中山大学生命科学学院为文章第一单位,我院博士后陈添琦,特聘副研究员孙雨蒙(现为南方医科大学副教授),博士生朱顺鑫为本论文的共通第一作者,我院陈月琴教授、王文涛副教授和中山大学附属第一医院黄礼彬主任为共同通讯作者。该研究得到国家重点研发计划、国家自然科学基金和广东省重大研究项目等项目的资助。
原文链接:
https://link.springer.com/article/10.1038/s44318-026-00707-1



